L'idea che tutte le sostanze nel mondo siano composte da atomi è nata nel V secolo a.C., quando l'antico pensatore greco Democrito suggerì che tutto ciò che esiste è composto dalle più piccole particelle mobili. Si potrebbe solo supporre che, molto probabilmente, non è privo di significato. Per molti secoli dopo Democrito, gli atomi venivano periodicamente richiamati, ma questa ipotesi non era popolare in quei tempi remoti. Nel diciannovesimo secolo, l'ipotesi atomica riapparve sull'orizzonte scientifico.
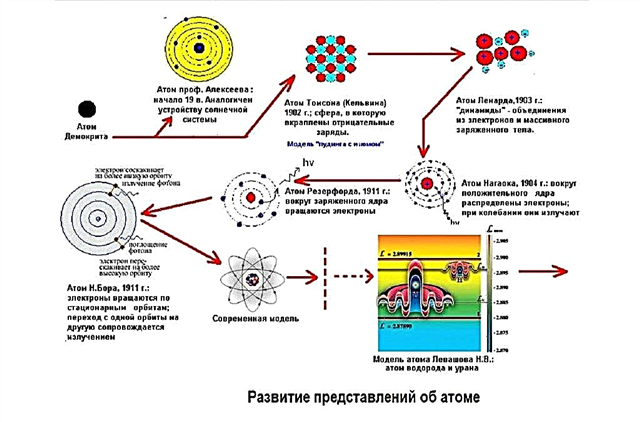
Modelli di struttura atomica

Gli scienziati erano alla ricerca di un modello in grado di descrivere in modo soddisfacente l'immagine del mondo reale. L'atomo si è rivelato un modello molto adatto. Sebbene gli atomi non possano essere visti, ma consentendo loro di esistere, gli scienziati potrebbero spiegare ciò che hanno osservato nei loro esperimenti e in natura.
Gli scienziati erano convinti dell'esistenza degli atomi molto prima che potessero provarlo. Il modello ha funzionato, sebbene nessuno potesse dimostrare la sua verità. Ad esempio, all'inizio del XIX secolo, lo scienziato inglese John Dalton, studiando le leggi delle reazioni chimiche, scoprì che due sostanze reagiscono sempre chimicamente nella stessa proporzione costante. Ad esempio, la combinazione di una parte di ossigeno e due parti di idrogeno fornisce acqua.
Ciò ha suggerito che gli atomi di una sostanza, uguali in massa tra loro, si sono uniti con gli atomi di un'altra sostanza (cioè con atomi di una massa diversa). Nel caso della formazione di acqua, un atomo di ossigeno si combina con due atomi di idrogeno.Il modello atomico ha aiutato a capire cosa osservò esattamente Dalton nei suoi esperimenti. Vi sono ulteriori prove semplici per l'esistenza di atomi.
Se guardi al microscopio le particelle di polline sospese nell'acqua, puoi vedere che fanno movimenti casuali. Perché? Gli scienziati hanno suggerito che ciò potrebbe essere dovuto al fatto che le particelle di polline si scontrano con numerosi atomi o gruppi di atomi che gli scienziati hanno chiamato molecole (ad esempio, le particelle nell'acqua si scontrano con molecole d'acqua).
In cosa consiste un atomo?
Gli scienziati che erano d'accordo con la teoria atomica credevano che un atomo fosse costituito da piccole particelle cariche elettricamente - positive e negative, che, se combinate in un atomo come in una palla, si neutralizzano a vicenda e rendono l'atomo nel suo complesso elettricamente neutro. Ma nel 1907, il fisico inglese Ernest Rutherford, con i suoi esperimenti, dimostrò che ciò non era del tutto vero.
Esperienza di Rutherford
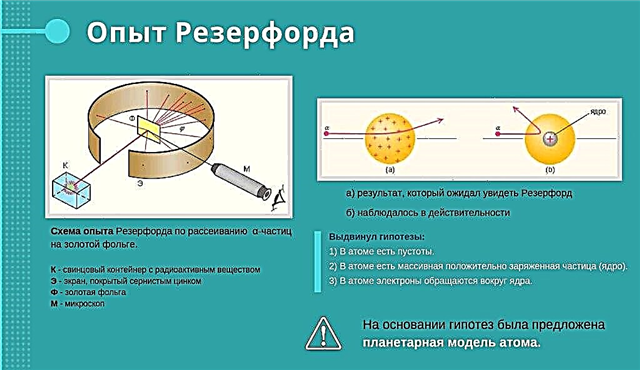
Rutherford bombardò una lamina d'oro con un raggio ad alta velocità di particelle cariche positivamente. Credeva che le particelle sarebbero passate attraverso la lamina. Alcune particelle caricate positivamente volarono attraverso la lamina. E alcuni non potevano farlo. Inoltre, rimbalzarono nello sperimentatore, come se una forza nascosta nel foglio li allontanasse. Rutherford fu sorpreso. Disse che era lo stesso che iniziare a bruciare la pentola su carta fibrosa e improvvisamente vedere come la pentola vola via dalla fronte del vasaio.
Modello atomico planetario - Atom Core
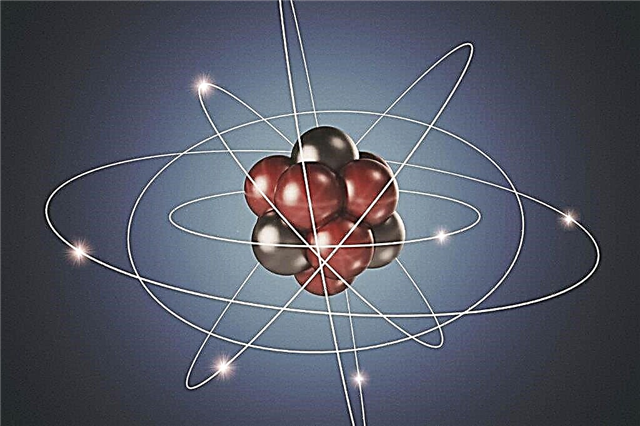
Gli esperimenti di Rutherford hanno contribuito a confermare l'ipotesi atomica e a capire come funziona l'atomo. È diventato chiaro che le particelle positive e negative non sono distribuite uniformemente nell'atomo. Se così fosse, le particelle caricate positivamente nell'esperimento di Rutherford non sarebbero respinte con tale forza. Quindi, il nucleo di un atomo non è neutro. Nel mezzo dell'atomo c'è una densa palla di particelle, cioè nel mezzo, che è chiamato il nucleo dell'atomo, sono protoni caricati positivamente e neutroni neutri.
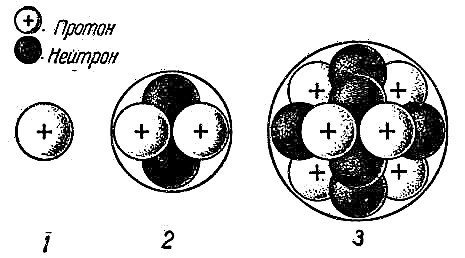
A una distanza considerevole dal nucleo, particelle cariche negativamente - elettroni - ruotano attorno alle sue orbite attorno ad esso. Poiché una carica positiva ha lo stesso valore di una carica negativa, l'atomo nel suo insieme è elettricamente neutro. Non comporta alcun addebito.
Ma il nucleo stesso è la concentrazione di una carica positiva. Molte delle particelle positive nell'esperimento di Rutherford volarono troppo vicino al nucleo carico positivamente di un atomo d'oro. Poiché le cariche positive si respingono a vicenda, queste particelle sono volate indietro verso lo sperimentatore. Questo gli ha spinto all'idea di come siano effettivamente disposti gli atomi.
I quark
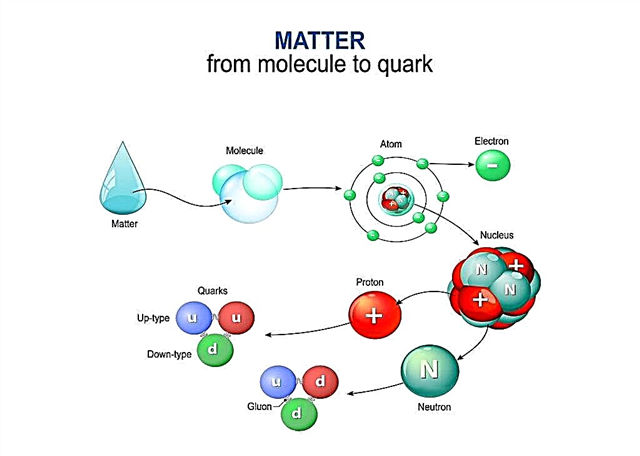
Protoni e neutroni sono particelle che, sebbene siano piccole, sono costituite da particelle ancora più piccole chiamate quark. Oggi gli scienziati credono che protoni e neutroni siano costituiti da particelle ancora più piccole chiamate quark.
I quark sono un nuovo modello che spiega meglio il comportamento degli atomi nel mondo reale. E proprio come gli scienziati avevano precedentemente cercato prove sperimentali sull'esistenza di atomi, ora stanno cercando una vera conferma dell'esistenza di quark.












